|
|
KİMYASAL BAĞLAR
Aynı ya da farklı cins atomları bir arada tutan kuvvetlere kimyasal bağlar denir.
Helyum, neon, argon gibi soy gazlar başka atomlarla bileşik yapmadan tek atom hâlinde bulunur. Soy gazların dışındaki diğer element atomları son yörüngelerindeki elektron sayısını soy gazlara benzetip kararlı hâle geçmek isterler. Bunun için de elektron alış ya da verişi gerçekleşir.
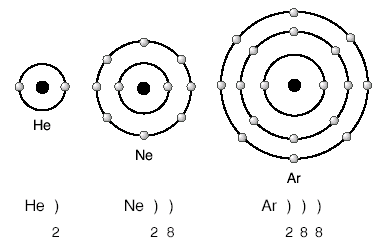
Örneğin; 11 elektronu olan Na, 1 e– vererek 10 elektronlu neona benzer. 3 elektronlu Li, 1 e– vererek helyuma benzer. 9 elektronlu F, bir e– alarak 10 elektronlu neona benzer.
1A, 2A ve 3A grubu elementleri (metaller) elektron vererek kararlılığa ulaşır. 5A, 6A, 7A grubu elementleri (ametaller) ise elektron alarak soy gazlara benzerler. Kimyasal bağlar iyonik ve kovalent olmak üzere ikiye ayrılır.
İyonik bağ:
(+) ve (–) yüklü taneciklerin (iyonların) arasında elektriksel çekim kuvvetiyle oluşan bağa iyonik bağ denir. İyonik bağ yapan atomlardan elektron veren (+) yüklü, elektron alan (–) yüklü iyon olur. Yemek tuzu, sodyum ve klor atomlarının iyonik bağ yapmasıyla oluşur. Atom numarası 11 olan sodyum (Na), atom numarası 17 olan klor`a (Cl) 1 elektron verir. Her ikisi de kararlı hale gelir. Aralarında iyonik bağ oluşur.
Sodyumun (Na) Na+ iyonuna dönüşmesi:
11 elektronlu sodyum atomu 1 elektron vererek kararlı hale gelir.
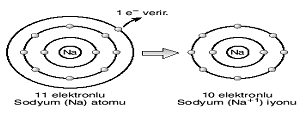
17 elektronlu klor atomu 1 e– alarak kararlı yapıya geçer.
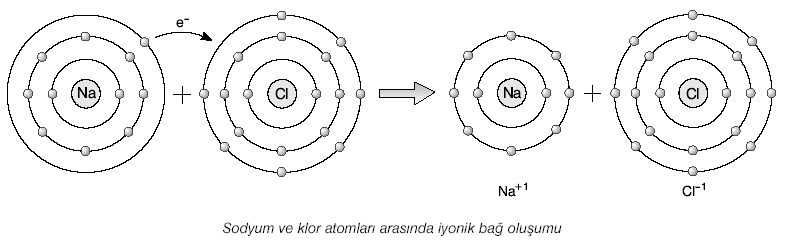
Sodyum ve klor atomları, arasında iyonik bağ yaparak NaCl bileşiğini oluşturur.
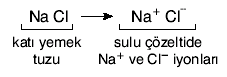
Na + Cl Na+1 + Cl–1 NaCl
İyonik bağ yaparak oluşan maddelere iyonik yapılı maddeler denir. Bir Metal ile bir ametal iyonik bileşik oluşturur.
İyonik bileşikler oda şartlarında genellikle katı hâlde ve kristal yapıda bulunur.
Sert ve kırılgan bir özelliğe sahiptir. İyonik kristaller katı hâlde elektrik akımını iletmez fakat sulu çözeltilerinde iyonlarına ayrışır ve elektrik akımını iletir.
Yemek tuzu iyonik bağlı bir bileşiktir ve kristal yapıdadır.
İyonik Bağlı Bileşiklerde Kristal Yapı
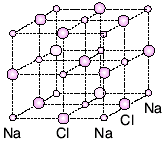
İyonik bağlı bileşiklerde iyonlar birbirini en kuvvetli şekilde çekecek bir düzen içinde dizilirler. Böyle düzenli birleşen atomlardan kristal yapı adını verdiğimiz düzgün geometrik şekiller oluşur. Yemek tuzunun kristal yapısı buna örnektir. Yemek tuzundaki (NaCl) kristal yapı, şekildeki gibidir.
 |
|
|
Bu konu 101790 kez okundu |
|
Bu konuyu Site Admini Ekledi |